目前,这一疗法的发展已进入快车道,从实验室的创新探索快步走进临床应用的新阶段。截至现在,全球范围内获批上市的CAR-T药物已达13款,其中已在国内获批上市的就有7款,适应症广泛覆盖白血病、淋巴瘤、多发性骨髓瘤等多种常见血液肿瘤类型。CAR-T细胞疗法在临床上的成功,将其从一项前沿技术推向了产业化应用的新阶段。然而,其产业化进程面临一个核心矛盾:高度个体化的制造流程如何实现规模化量产?本文将系统分析制造瓶颈的根源,并探讨以"质量源于设计"为核心的解决方案。
制造瓶颈的根源:复杂流程与系统性变量
CAR-T疗法的制造流程具有高度复杂性和环环相扣的特点。以典型的临床规模自体CAR-T疗法为例,其制造始于患者体内的细胞采集,之后需历经T细胞激活、CAR基因转导、体外扩增等一系列精密操作,最终才能将成品细胞回输至患者体内。
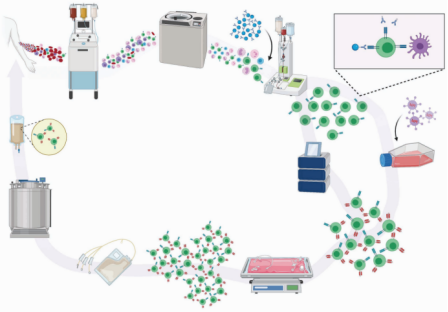
这一制造过程中的每个环节都对生产环境、操作规范和质量控制提出了极为严苛的要求,也使得整个生产体系在面对规模化需求时异常脆弱,其稳定性受到四大核心可变性挑战的严峻考验。这些挑战相互关联,共同直接决定了最终产品的质量、安全性以及不同生产批次间的一致性。
l操作可变性:依赖人员经验与开放工艺,不同操作人员手法、判断标准及设备参数偏差易引发失误与污染,导致批次失败及成本损失。
l原料与试剂可变性:CAR-T 细胞性能依赖培养基等关键试剂,但相关试剂缺乏全面标准化,不同厂家、批次效能有差异,且供应链可能受产能、物流影响中断,直接影响产品有效性与批次一致性。
l环境可变性:CAR-T 细胞对生产微环境敏感,温度、洁净度、气体张力等参数波动会影响细胞代谢、无菌性及质量(如温度失控致细胞活力下降)。
l生物因素可变性:患者个体异质性导致起始材料(单采血)中 T 细胞含量、亚群组成等存在差异,辅助细胞比例也各不相同,制约 CAR-T 细胞转导与扩增效果,是批间差异的根本原因之一。优化预处理工艺可部分缓解,但起始材料 “标准化” 仍是行业核心难题。
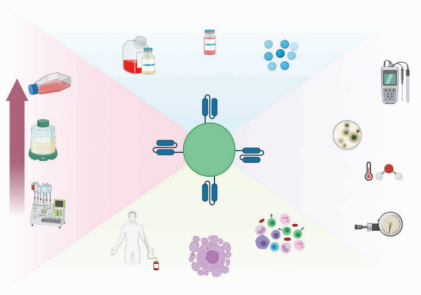
QbD原则下的制造革新:友康生物FEP细胞培养袋的系统性实践
面对上述挑战,行业共识在于必须将“质量源于检验”升级为“质量源于设计”(Quality by Design, QbD)的前瞻性设计理念。作为这一变革的践行者,友康生物通过FEP细胞培养袋的创新研发,将QbD理念深度融入产品设计的每个环节,为行业提供了一套系统性的解决方案。
1、目标导向的质量设计:以材料创新奠定质量基石
QbD原则要求在产品开发初期就明确关键质量属性。基于这一理念,友康生物在材料选择阶段就确立了以"化学稳定性、生物相容性、工艺适应性"为核心的质量目标,以此作为克服传统材料局限、满足高标准细胞培养需求的基石。
传统材料的局限性与创新材料的突破:传统EVA材料在透气性、保水性等方面的局限,使其难以满足高标准细胞培养的需求。而友康生物采用的FEP(全氟乙烯丙烯共聚物)材料,为100%惰性材质,单层高纯度材料,在加工过程中不添加任何增塑剂和其他生物源材料,因此在生物相容性上有非常优异的表现,满足USP Class VI(美国药典生物相容性检测最高级别)的要求。
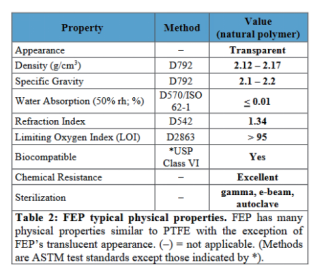
FEP材料的多重技术优势与应用价值:在实际应用中,FEP材料凭借其高透明度(透光率高达95%)与低表面能特性(18 dyn/cm),在细胞培养过程中实现了非侵入式实时观测、有效抑制生物膜形成、显著减少培养液蒸发损失并防止成分吸附等多重优势,共同保障了培养环境的稳定性和结果的可预测性。另外,-80℃至200℃的宽温度范围,不仅支持多种灭菌方式的选择,也为运输和储存过程中的温度波动提供了安全余量。
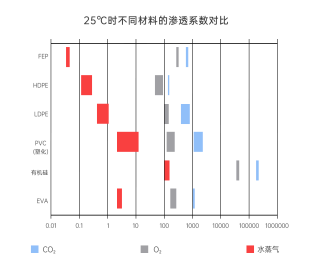
2、风险驱动的参数控制:构建全过程质量防护体系
在QbD框架下,对关键工艺参数的识别和控制至关重要。友康生物通过系统性的风险评估,将可能影响产品质量的因素纳入设计考量,建立起多层次的物理与性能防护体系。
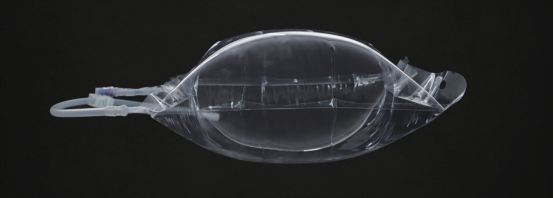
物理屏障:物理屏障设计是风险控制的首要环节。培养袋采用全封闭结构,配备经过严格验证的无菌接口,有效杜绝了外界污染源的侵入。
机械性能:该培养袋在限高测试中可承受59 kPa的内部充气压力且无泄漏;在不限高条件下,即使加压至15 kPa导致袋体明显膨胀变形,四周焊缝仍保持完好,无泄漏点,展现出优良的机械强度与密封可靠性。

3、全链条的质量贯穿:从原材料到终端用户的完整保障
QbD原则强调质量要求必须贯穿从原材料采购到最终使用的全过程。友康生物通过建立完善的质量管理体系,实现了从“产品供应商”到“质量合作伙伴”的角色升华。
l智能生产与严格质控:公司依托4.2万平方米的智能化生产基地,在B+A级洁净环境下严格执行GMP标准。结合48项专利技术和ISO13485质量体系认证,为产品的高度一致性和可靠性提供了坚实的制度与硬件保障。
l稳定的供应链与完善的技术支持:通过建立稳定的物料采购渠道,确保了供应的连续性与可靠性。此外,友康生物还提供完整的研究数据,这些经过严格验证的技术资料为用户的产品申报和工艺转移提供了强有力的支持,真正体现了QbD原则在全链条质量管理中的具体实践。
总结
CAR-T细胞疗法是肿瘤治疗领域的里程碑。以QbD原则为核心,推动生产系统向功能封闭转型,并实现关键耗材的材料升级,是解决制造可变性、惠及更多患者的必由之路。通过推动从手工操作到自动化、封闭化生产的系统升级,行业正致力于突破制造瓶颈,迈向更安全、有效、可及的CAR-T细胞治疗新时代。

 友康生物
友康生物 2025-12-09
2025-12-09 行业热点
行业热点



