细胞治疗产品正加速从实验室走向临床,产业化对规模化、标准化交付提出了更高要求。冻存成为连接生产与应用的必经环节,与细胞直接接触的冻存液,其安全性直接关系到产品质量与患者回输安全。2026年5月1日,《生物医学新技术临床研究和临床转化应用管理条例》(国务院第818号令)将正式施行,细胞治疗领域的监管红线将进一步收紧。冻存液的选择已不仅是技术参数的比较,更直接影响到IND审评与临床安全。
一、为何行业加速转向“三无”冻存液?
传统冻存液的核心风险主要来自三类长期被广泛使用的成分,它们在带来冻存保护的同时,也引入了显著的申报与安全性不确定性。

随着国内外监管对非必要动物源成分与高风险辅料的容忍度下降,上述风险正面临更严格的审视。
需要特别指出的是,二甲基亚砜(DMSO)除了已知的细胞毒性外,还可能干扰间充质干细胞的定向分化方向,例如诱导非预期的细胞类型分化或降低其多向分化潜能。
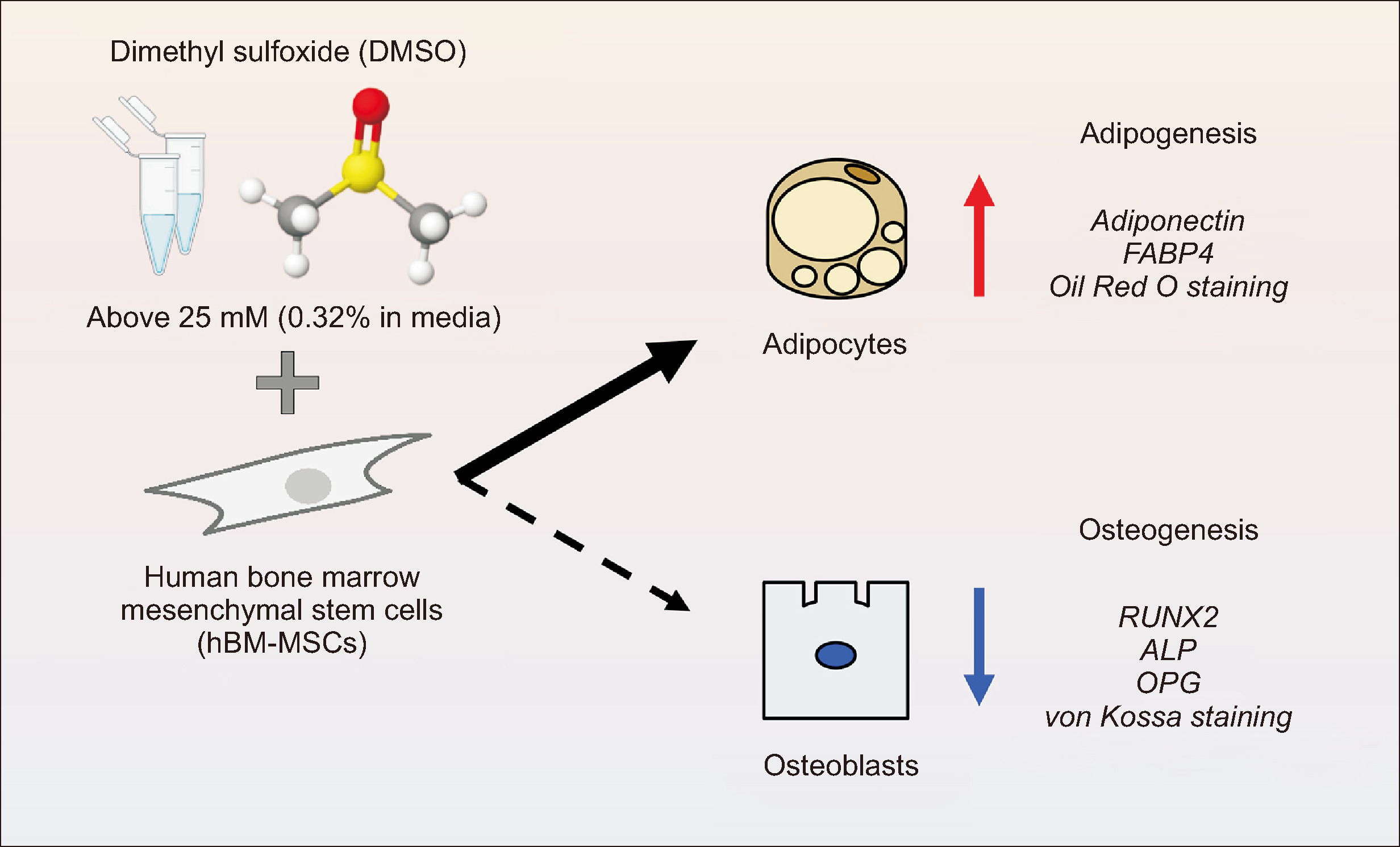
尽管在部分基础研究中 DMSO 也被用作分化促进剂,但这种浓度与细胞类型依赖的“双面性”,恰恰增加了其在干细胞药物中作为冻存保护剂的不确定性。对于需要精确维持干细胞特性的 MSC 药物而言,无 DMSO 方案正成为更审慎的选择。
基于上述考虑,“无血清、无蛋白、无DMSO” 的冻存液,凭借明确的成分定义与更高的安全边界,正从早期的“加分项”迅速转变为药企降低申报不确定性、提升合规水平的优先选择。
二、友康“三无”冻存方案的进阶路线:从申报背书到生产适配
友康生物基于多年无血清培养基研发经验,推出三款覆盖不同应用场景的“无血清、无蛋白、无DMSO”细胞冻存液——NC1010(成熟申报案例)、NC1011(高性能与便利性)、NC0606(大规模生产)。三款产品成分明确,GMP级生产,符合药用辅料标准。以下分别介绍各款产品的完整信息。
第一代:GMP级细胞冻存液(NC1010)—— 具备成熟申报案例的方案
NC1010是友康生物于2018年推出的第一款无蛋白、无DMSO、无血清的GMP级冻存液,专门为细胞药物生产而设计,已成功伴随客户药物进入中美双报临床Ⅱ期,并完成 FDA 备案(MF 29496),是“有案例可循”的稳妥选择。
产品优势:
成分特点:无血清、无蛋白、无DMSO,所有成分均明确。
合规资质:遵循 GMP 生产规范,全程无菌控制,产品经过严格质量检测。
性能优势:复苏后细胞活率>90%,已完成急性毒性实验。
核心亮点:有明确申报案例,已关联药品进入中美双报临床Ⅱ期。友康可协助客户进行细胞药物申报中关于冻存液部分工作的指导。
性能验证:
GMP级细胞冻存液在长期冻存中能更好地维持细胞活性,细胞存活率整体优于传统细胞冻存液。
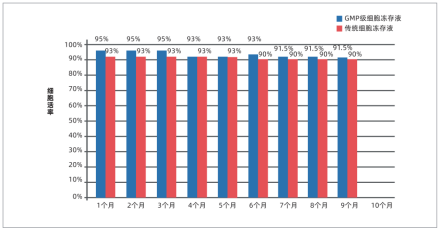
MSC细胞冻存时间与复苏活率对照
操作要点:
冻存前需使用程序降温盒,逐步降温后投入液氮。
复苏后需用培养基离心清洗,去除冻存液后再接种。
适用对象及场景:
项目已进入或即将进入临床申报,需要一个“有申报先例”的冻存液。适用于间充质干细胞。
第二代:GMP级玻璃化细胞冻存液NC1011——高性能与便利性兼顾的升级方案
NC1011是友康生物在NC1010基础上推出的升级产品,引入玻璃化冻存技术,并完成中美双备案,在保持高安全性的同时大幅提升冻存效果与操作便利性。

产品优势:
成分特点:无血清、无蛋白、无DMSO,所有成分均明确,冻存液本身可在常温中保存,大大降低运输保存成本。
技术特性:采用玻璃化冻存技术,高浓度保护剂快速固化细胞内液,避免冰晶形成,实现超快速冻存。
性能优势:细胞复苏活率稳定达90%以上,细胞回收率高于传统冻存液。
核心亮点:拥有NMPA药用辅料备案(F20250000077)与FDA DMF备案(37754),中美双报路径清晰。
性能验证:
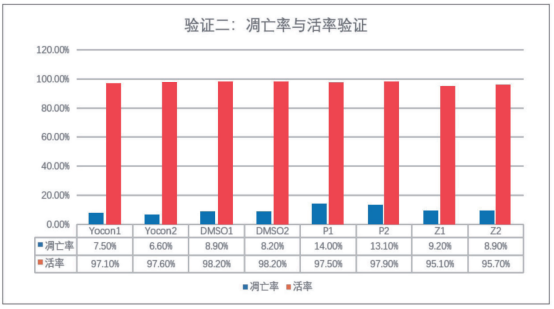
细胞复苏活率可稳定维持在接近100%水平,细胞复苏率略高于DMSO冻存液,远高于进口成品冻存液。
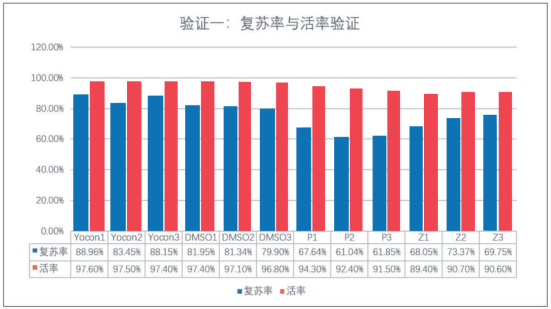
操作要点:
无需程序降温,重悬后直接转移至-80℃冰箱,过夜后转液氮。
复苏后无需离心清洗,可直接接种。
适用对象及场景:
准备IND申报,需要明确药用辅料资质,追求高复苏率与操作便利性。适用于间充质干细胞(脐带、脂肪等来源)。
第三代:低渗MSC细胞冻存液(NC0606)—— 面向大规模生产的专用方案
NC0606是友康生物最新开发的低渗MSC细胞冻存液,专为大规模生产场景设计,提供40分钟室温操作窗口和低渗配方。

产品优势:
成分特点: 无血清、无人源、无动物源、无DMSO、无蛋白,所有成分均明确,GMP级生产,避免细胞毒性与临床应用风险。
技术特性: 采用低渗配方(渗透压850-950 mOsm/kg),降低回输后局部组织水肿风险;细胞可在冻存液中室温稳定保存40分钟,为大规模灌装线操作提供充足时间窗口。
性能优势:冻存MSC活率均>90%;冻存1个月后复苏率仍超90%,扩增倍数稳定,细胞增殖能力不受影响。
核心亮点: 专为MSC药物制剂大规模生产设计,兼顾工艺便利性与细胞安全性,性能表现优异。
性能验证:
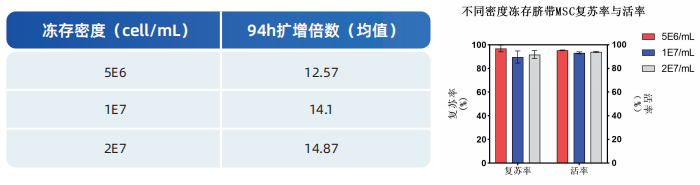
以三个密度梯度冻存脐带MSC细胞,复苏率与活率均>90%,3-4天细胞扩增倍数>10倍。
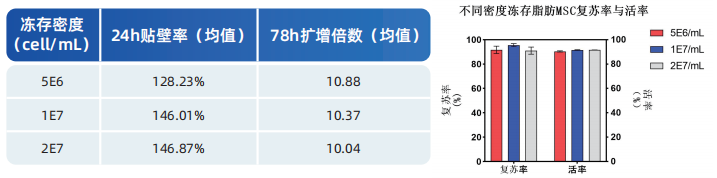
以三个密度梯度冻存脂肪MSC细胞,复苏率>85%,活率>90%,24h贴壁率>100%,3-4天细胞扩增倍数>10倍。
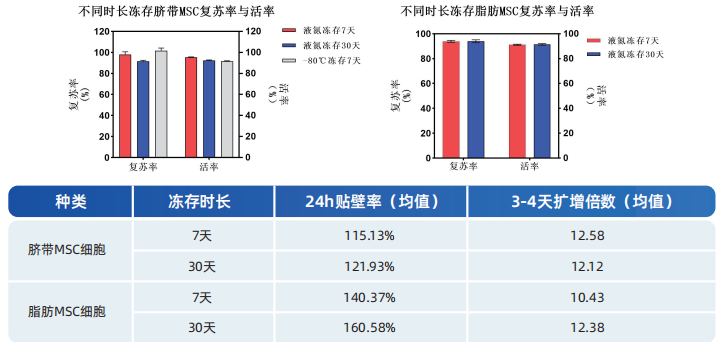
该冻存液在短期冻存(数天内)与长期冻存(1个月内)对不同来源的MSC均能维持高复苏率与活性,且细胞增殖能力不受影响。
操作要点:
无需程序降温,重悬后直接转移至-80℃冰箱,过夜后转液氮。
复苏后无需离心清洗,可直接接种。
适用对象及场景:
从事MSC药物研发、生产,尤其是有大规模灌装需求的客户;申报需求不急迫或可同步推进。适用于人间充质干细胞(脐带、脂肪等来源)。
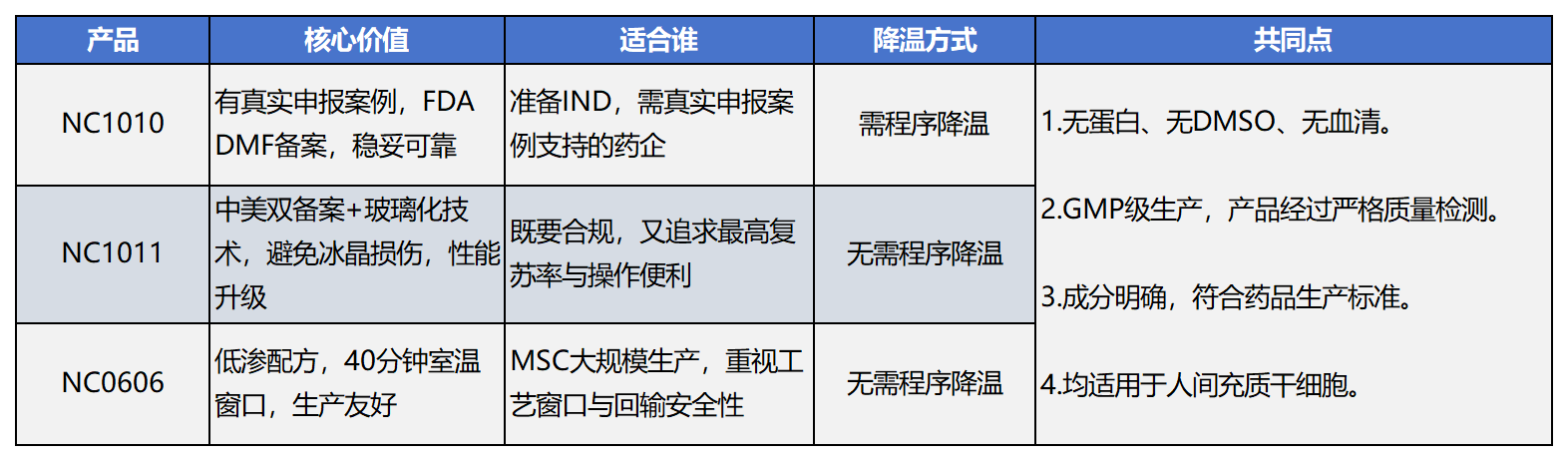
三、选型总结:一张表匹配你的场景
YOCON
在818号令即将实施的背景下,冻存液的选型本质是“为产品安全加锁”。与其在申报后期被动解释传统辅料的风险,不如在研发前端主动选择合规、安全、有数据支撑的方案。友康生物的三款无蛋白冻存液,分别针对申报背书、性能升级、大规模生产三个关键场景,提供了经过验证的合规选择。如果您正处于IND申报的关键阶段,或正在优化生产工艺,不妨从这三款产品中找到最适合您的那一款。


 2026-04-22
2026-04-22 公司热点
公司热点



